W przepisach unijnych istnieją pewne odstępstwa w tym zakresie, dotyczące etykietowania naturalnych wód mineralnych i żywności dla szczególnych konsumentów, jednak co do zasady wszelkiego rodzaju stwierdzenia bądź sugestie dotyczące właściwości leczniczych są niedozwolone tak w znakowaniu, prezentacji, jak i reklamie żywności.
Kwestie rozróżnienia pomiędzy cechami właściwymi dla żywności i produktów leczniczych były przedmiotem wielu konsultacji i postepowań (włącznie z sądowymi), zarówno na poziomie krajowym, jak i unijnym. Pomimo ugruntowanej linii orzeczniczej i wielu przewodników kierowanych do przemysłu, bez trudu można znaleźć na rynku produkty (w szczególności suplementy diety), oznakowane lub reklamowane w sposób sugerujący właściwości leczenia lub zapobiegania chorobom.
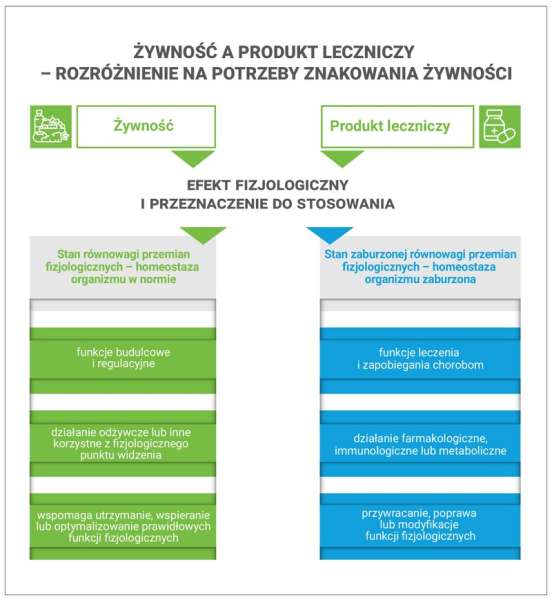
Dokumentem pomocnym dla przedsiębiorców w rozróżnieniu cech żywności i produktów leczniczych mogą być wytyczne Rady Europy z 2008 r., przygotowane przez Komitet Ekspertów ds. Żywienia, Żywności i Zdrowia Konsumentów (Grupa ds. Suplementów Diety). W opracowaniu tym eksperci przedstawiają kwestie problemowe na przykładzie modelu homeostazy. Zgodnie z tym opracowaniem jedynie produkty lecznicze mają zdolność przywracania homeostazy do stanu równowagi. Eksperci wskazują, że dwa zasadnicze kryteria jakie należy stosować w rozróżnieniu pomiędzy suplementem diety (żywnością), a produktem leczniczym to przeznaczenie do stosowania, oraz rodzaj wywołanego efektu, oceniany na podstawie jednego lub większej liczby parametrów fizjologicznych.
Żywność a produkt leczniczy – rozróżnienie na potrzeby znakowania żywności
Uwzględniając powyższe zgodnie z opinią Rady, produkt może być uznany za leczniczy ze względu na „prezentację” lub „funkcję”. Zgodnie z utrwalonym orzecznictwem pojęcie „prezentacja” produktu powinno być interpretowane w sposób rozszerzający. Produkt należy uznać za „przedstawiony jako mający właściwości leczenia lub zapobiegania chorobom u ludzi” w rozumieniu Dyrektywy 2001/83 (dot. produktów leczniczych), gdy jest w ten sposób wyraźnie „określony” lub „zalecany”, np. na etykiecie, ulotce lub w przekazie ustnym. Pojęcie „przedstawienia” również powinno być interpretowane rozszerzająco (takie stanowisko zajął Trybunał Sprawiedliwości w wyroku w sprawie 227/82 Van Bennekom). Kryterium przedstawienia będzie spełnione zawsze gdy przeciętnie poinformowany konsument, nawet w sposób domyślny, ale z pewnością odnosi wrażenie, że produkt ten, biorąc pod uwagę jego opakowanie, ma odpowiednie właściwości. Przy dokonywaniu oceny należy wziąć pod uwagę perspektywę przeciętnie poinformowanego konsumenta, u którego określona forma produktu może wzbudzić zaufanie (np. tabletka). Zaufanie zwykle wzbudzają również produkty lecznicze ze względu na gwarancje związane z ich wytwarzaniem (np. „wyprodukowane w standardzie farmaceutycznym”) i sprzedażą (apteka). Wprawdzie forma zewnętrzna określonego produktu może być ważną wskazówką przemawiającą za jego kwalifikacją, jako produktu leczniczego wedle sposobu prezentacji, jednak forma ta dotyczy nie tylko samego produktu, ale również jego opakowania.
Dodatkowo z orzeczeń sądów krajowych wynika, że często samo wskazanie jednostki chorobowej w prezentacji lub reklamie żywności będzie uznane za sugestię korzystnego oddziaływania tej żywności (lub jej składników) na poprawę stanu zdrowia w danej chorobie. Również może być uznane wskazanie do stosowania tej żywności w przypadku określonych jednostek chorobowych. W konsekwencji powyższego wszelkiego rodzaju sugestie odnoszące się do poprawy lub wspierania stanu zdrowia w konkretnych jednostkach chorobowych – wymienionych w Międzynarodowej Klasyfikacji Chorób i Problemów Zdrowotnych ICD 10 – mogą być przedmiotem zastrzeżeń organów urzędowej kontroli żywności.
Wyjątek mogą stanowić jednak oświadczenia zdrowotne odnoszące się do zmniejszenia ryzyka choroby, o których mowa w rozporządzeniu 1924/2006. Oświadczenia o zmniejszaniu ryzyka choroby to kategoria oświadczeń stanowiących o tym, że spożycie określonej żywności lub zawartego w niej składnika znacząco zmniejsza jakiś czynnik ryzyka w rozwoju choroby dotykającej ludzi.
Przykład: niska gęstość mineralna kości stanowi czynnik ryzyka w odniesieniu do osteoporotycznych złamań kości u kobiet w okresie pomenopauzalnym. Wapń pomaga zmniejszyć utratę minerałów kostnych zmniejszając tym samym ryzyko złamań. Jednak nie oznacza to, że spożycie określonej ilości wapnia zapobiegnie osteoporozie lub zagwarantuje pełnię zdrowia układu kostnego przez całe życie – jak sugerują niektóre, nieprawidłowe przekazy reklamowe.
Bez względu na przekonanie o wpływie żywności lub jej składników na zdrowie, przedsiębiorcy branży spożywczej – przy etykietowaniu (np. opakowania, ulotki), prezentacji (np. strony internetowe, targi żywności), a także w reklamie żywności (w tym kierowanej do specjalistów w zakresie zdrowia np. lekarz, farmaceuta) – muszą pamiętać, że przepisy prawa żywnościowego (poza ściśle określonymi w przepisach przypadkach) nie zezwalają na przypisywanie jej cech leczenia lub zapobiegania chorobom. Konsekwencją naruszania ww. regulacji mogą być nie tylko kary za niewłaściwe znakowanie lub reklamę, ale również za naruszanie zbiorowego interesu konsumentów.
Warto podkreślić, że rozwiązaniem służącym zwiększeniu atrakcyjności produktów przewidzianym w przepisach unijnych jest ustanowienie systemu autoryzacji oświadczeń zdrowotnych, który daje firmom możliwość zdobycia przewagi konkurencyjnej.
Homeostasis a model to distinguish between foods (including food supplements) and medicinal products. Council of Europe (07.02.2008).